Физический энциклопедический словарь - диаграмма состояния (диаграммаравновесия фазовая диаграмма)
Диаграмма состояния (диаграммаравновесия фазовая диаграмма)
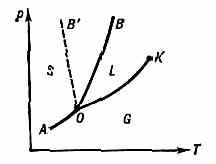
Обычно рассматривают проекции трёхмерной Д. с. на одну из координатных плоскостей (чаще на плоскость р, Т', рис.). Любая точка Д. с. (ф и г у р а т и в н а я т о ч к а) изображает равновесное состояние в-ва при данных значениях р и Т. Точка О (тройная точка) соответствует равновесию трёх фаз в-ва: твёрдой, жидкой и газообразной. В точке О пересекаются три кривые: ОА (кривая в о з г о н к и, или сублимации), каждая точка к-рой соответствует равновесию тв. и газообразной фаз в-ва; ОК (кривая испарения) — жидкой и газообразной фазам; кривая плавления 0В (или ОB') — тв. и жидкой фазам (OS для в-в, у к-рых темп-ра плавления Тпл растёт с давлением, OB' для в-в с уменьшающейся Тпл с ростом р). Эти кривые делят плоскость Д. с. на области существования каждой из трёх фаз: твёрдой (S), жидкой (L) и газообразной (G). В точке K — критической точке исчезает различие между св-вами жидкости и газа. Согласно Гиббса правилу фаз, точке О соответствует безвариантное равновесие, точкам на кривых ОА, ОВ (ОB') и ОК — моновариантное равновесие, а точкам в каждой из областей S, L и G — дивариантное (двухвариантное) равновесие. При существовании у в-ва полиморфных модификаций Д. с. усложняется (число тройных точек равно числу полиморфных превращений, см. Полиморфизм).
Для построения Д. с. используют данные термич. анализа, рентгеновского
структурного анализа, оптич. и электронной микроскопии, нейтронографии, дилатометрии, измерений твёрдости и др. методов.
• Аносов В. Я., Краткое введение в физико-химический анализ, М., 1959; В о л А. Е., Строение и свойства двойных металлических систем, т. 1—2, М., 1959—62; В о л А. Е., К а г а н И. К., Строение и свойства двойных металлических систем, т. 3, М., 1976; П е т р о в Д. А., Тройные системы, М., 1953; Воловик Б. Е., Захаров М. В., Тройные и четверные системы, М., 1948; П а л а т н и к Л. С., Л а н д а у А. И., Фазовые равновесия в многокомпонентных системах, Хар., 1961.

Вопрос-ответ:

Похожие слова
Самые популярные термины
1 | 1384 | |
2 | 1053 | |
3 | 995 | |
4 | 944 | |
5 | 926 | |
6 | 829 | |
7 | 803 | |
8 | 802 | |
9 | 713 | |
10 | 711 | |
11 | 691 | |
12 | 638 | |
13 | 628 | |
14 | 615 | |
15 | 533 | |
16 | 525 | |
17 | 518 | |
18 | 502 | |
19 | 484 | |
20 | 480 |









